前言
我國每年有大量的重金屬廢水產(chǎn)生���,而中和沉淀法是處理此類廢水的重要方法之一[1]���。但是,該方法在處理廢水后會產(chǎn)生大量的重金屬廢渣���。此類重金屬廢渣又稱中和渣���,具有產(chǎn)量大、含水率高���、成分復(fù)雜等特點���,處理處置比較困難。同時���,隨著天然資源的不斷開發(fā)和利用���,重金屬天然礦資源日趨枯竭,人們越來越重視從固體廢棄物中回收重金屬資源[2]���。硫化浮選技術(shù)是近年來研究的新方法之一[3-6]���。從世界范圍來看���,目前絕大部分鋅、鉛等金屬是從硫化礦中提取出來的���,如果將廢渣中的重金屬轉(zhuǎn)化為可浮性好的金屬硫化物���,便可以運用成熟的浮選工藝對其進(jìn)行回收,是一種重金屬廢渣資源化的新方法���。硫化浮選工藝不僅轉(zhuǎn)化率高���、成本較低,處理后的廢渣化學(xué)性質(zhì)穩(wěn)定;同時���,采用該技術(shù)回收的金屬硫化礦可以直接進(jìn)入現(xiàn)有的冶煉系統(tǒng)���,因此對現(xiàn)有的冶煉系統(tǒng)的技術(shù)改造成本相對較低。
目前���,采用硫化鈉等溶液進(jìn)行硫化的方式應(yīng)用較廣[7,8]���,但是硫化鈉在使用過程中容易產(chǎn)生硫化氫等有毒氣體,容易產(chǎn)生二次污染;同時���,越來越多的研究發(fā)現(xiàn)���,人工轉(zhuǎn)化而成的重金屬硫化物在表面性質(zhì)、晶體結(jié)構(gòu)���、粒度大小等方面與天然硫化礦存在一定差異���,會對后續(xù)的浮選產(chǎn)生不利影響[9]。因此如何提高人造硫化的可浮性是現(xiàn)有硫化技術(shù)的難點之一���。根據(jù)地質(zhì)學(xué)和礦物學(xué)理論���,結(jié)晶性好的天然硫化礦是在水熱條件下形成的[10]。因此���,采用水熱硫化技術(shù)不僅能保證較高的硫化率���,同時可以對形成的人造硫化物晶體進(jìn)行調(diào)控[11-13]���,容易得到結(jié)晶性與天然礦物相似、易于浮選的重金屬硫化物���,從而實現(xiàn)重金屬的高效回收���。
然而,目前水熱硫化技術(shù)一般運用于特種功能性材料的制備���,將此類技術(shù)運用于重金屬廢渣的資源化處理的報道較少���。本文以前期的文獻(xiàn)調(diào)研和探索試驗研究為基礎(chǔ),對含鋅等重金屬廢渣水熱硫化工藝的過程特征及反應(yīng)機(jī)制進(jìn)行探討���。本文作者首先通過熱力學(xué)計算���,繪制出水熱條件下S-H2O的Eh-pH圖,開展水熱體系下硫元素賦存狀態(tài)的研究;隨后���,本研究結(jié)合X射線衍射圖譜���,對水熱硫化的反應(yīng)過程進(jìn)行探討;最后���,本文還對水熱條件下硫化鋅晶體的晶體結(jié)構(gòu)和生成規(guī)律進(jìn)行探討。通過開展上述三個方面的基礎(chǔ)研究���,為重金屬廢渣水熱硫化回收金屬工藝提供研究基礎(chǔ)和科學(xué)依據(jù)。
1 實驗
1.1 實驗材料
實驗所用重金屬廢渣主要來源于我國株洲冶煉廠廢水處理工段所產(chǎn)生的廢水中和渣���。通過添加石灰���、生物制劑等藥劑后,廢水中的重金屬離子變?yōu)槌恋砦锩摮?��,沉淀物?jīng)過濃縮���、脫水后便得到所謂的廢水中和渣。實驗將采集的廢渣樣本烘干后���,研磨過200目篩���,備用���。廢渣中具體化學(xué)成分如表1所示。結(jié)果表明���,廢渣中鋅���、鉛等重金屬含量較多,除此之外還含有一定量的Ca等元素���。
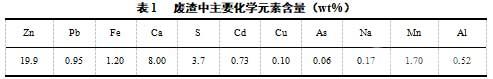
除外���,試驗還以重金屬氫氧化物和單質(zhì)硫磺為主要原料,模擬廢渣反應(yīng)體系���,在水熱過程中制備出了純的重金屬硫化物���,并對該人造硫化物的晶體結(jié)構(gòu)和生長規(guī)律進(jìn)行了研究。
1.2 實驗過程和分析方法
本文從水熱體系下硫元素賦存狀態(tài)���、中和渣水熱硫化過程特征以及水熱合成硫化鋅晶體結(jié)構(gòu)及生長規(guī)律的研究三個方面開展相關(guān)的基礎(chǔ)理論研究���。各部分的實驗過程和分析方法如下���。
1.2.1水熱體系下硫元素賦存狀態(tài)的研究
本研究主要采用HSC chemistry5.0對S-H2O的Eh-pH圖進(jìn)行繪制。
1.2.2中和渣水熱硫化過程的研究
水熱硫化實驗以GCF-1L系列強(qiáng)磁力回轉(zhuǎn)攪拌反應(yīng)釜為反應(yīng)設(shè)備���,根據(jù)前期研究結(jié)果���,中和渣的最優(yōu)參數(shù)確定如下:硫磺添加量為15%,礦漿濃度為300g/L���,改變水熱硫化的反應(yīng)溫度和反應(yīng)時間,反應(yīng)結(jié)束后自然冷卻���,取出洗滌過濾烘干���。反應(yīng)不同時間下的樣品經(jīng)X射線衍射分析(XRD, D/max 2550 VB + 18 KW)。
1.2.3 水熱合成硫化鋅晶體結(jié)構(gòu)及生長規(guī)律的研究
為了研究人工合成人造硫化物晶體生長規(guī)律���,試驗?zāi)M中和渣水熱硫化條件���,以純金屬氫氧化物(Zn(OH)2)為原料,在不同反應(yīng)溫度和時間下制備出了硫化鋅晶體,并通過XRD進(jìn)行分析���,對其不同晶面的晶粒尺寸大小進(jìn)行計算���。晶粒尺寸以謝樂公式進(jìn)行計算[14]:
其中D為所得到的平均晶粒(nm),λ為X射線的波長���,B為各晶面特征峰的半峰寬���,θ為衍射角。其中B���、θ的數(shù)值通過Jade 5.0軟件對原XRD圖譜擬合后得出���。
2 結(jié)果與討論
2.1 水熱體系下硫元素賦存狀態(tài)的研究
水熱過程中硫元素各類賦存形態(tài)主要是由于硫磺的歧化反應(yīng)產(chǎn)生的(式2)。水熱體系下硫元素賦存狀態(tài)對整個體系的硫化過程會產(chǎn)生很重要的影響���,因此本研究繪制了不同溫度下(25℃和200℃)S-H2O的Eh-pH圖(圖1和圖2)���。通過圖1可以看出,由于S2O32-化學(xué)性質(zhì)不穩(wěn)定���,因此會進(jìn)一步轉(zhuǎn)化為SO42-;同時���,根據(jù)檢測���,實驗采用的廢渣體系的pH值在8.5-11之間,因此水熱過程中硫元素主要以S2-���、HS-���、SO42- 等形式存在,其中起硫化作用的主要是HS-���。同時,研究還認(rèn)為高溫下重金屬更容易被硫化���。這主要是因為高溫下���,硫化能力較強(qiáng)的硫離子可以存在于更加廣泛的pH范圍中。圖1和圖2表明���,在常溫下���,硫離子只可能穩(wěn)定存在于pH大于13的溶液體系中���,大部分的硫離子會以HS-存在�����,而根據(jù)熱力學(xué)分析���,硫離子的硫化能力比硫氫根離子的硫化能力強(qiáng)很多(式3、式4);但是當(dāng)溫度升高至200℃時���,硫離子可以存在于更加廣泛的pH范圍中(10.3-14)��,因此整個離子體系的硫化能力更強(qiáng)���。除此之外,研究認(rèn)為��,硫磺歧化反應(yīng)產(chǎn)生的大量SO42-會使反應(yīng)體系的pH降低��,不利于反應(yīng)的進(jìn)一步發(fā)生�����,因此水熱過程必須保證廢渣中含有足量含鈣類物質(zhì)與硫酸根離子進(jìn)行結(jié)合。
2.2 中和渣水熱硫化過程的研究
為了研究中和渣水熱硫化反應(yīng)的過程特征��,我們對不同水熱溫度和硫化時間下的中和渣水熱硫化產(chǎn)物進(jìn)行了XRD分析���。
圖3為反應(yīng)時間為1小時�����,在不同水熱溫度下得到的樣品的XRD圖譜��。從圖中可以看出���,當(dāng)反應(yīng)溫度升高至210℃時,廢渣中才開始出現(xiàn)硫化鋅的特征峰���,而當(dāng)反應(yīng)溫度繼續(xù)升高至250℃時���,硫化鋅的特征峰愈加尖銳�����,說明廢渣中鋅的硫化最優(yōu)溫度范圍在210℃以上���,升高溫度有利于硫化鋅晶體的生成��。此外�����,渣中的含鈣化合物也會隨著溫度發(fā)生變化���。圖3表明���,當(dāng)反應(yīng)溫度升高至250℃時,廢渣中的主要含鈣物質(zhì)由二水硫酸鈣轉(zhuǎn)化為硫酸鈣�����。由于硫酸鈣較二水硫酸鈣具有更強(qiáng)的膠凝性[15]�����,因此可以考慮利用浮選尾礦制備膠凝材料��,實現(xiàn)浮選尾礦的資源化利用��。
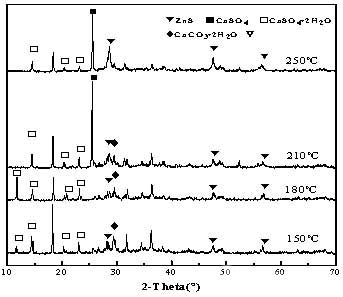
圖3 不同水熱溫度下硫化1h的中和渣的XRD圖
圖4為210℃下水熱硫化不同時間的中和渣的XRD圖譜��。結(jié)果表明,當(dāng)反應(yīng)1小時��,硫磺的歧化反應(yīng)已經(jīng)進(jìn)行�����,表現(xiàn)為硫磺的特征峰已經(jīng)完全消失;同時���,反應(yīng)產(chǎn)物中開始出現(xiàn)CaSO4的特征峰�����,而硫化鋅的峰不是很明顯���,說明硫酸鈣晶體的生成早于硫化鋅晶體的生成。反應(yīng)2小時后�����,硫酸鈣的特征峰進(jìn)一步加強(qiáng)��,中和渣中的二水硫酸鈣幾乎全部轉(zhuǎn)化為硫酸鈣�����,同時XRD圖譜上開始出現(xiàn)較明顯的硫化鋅的特征峰���。4h和8h的XRD圖譜中各物質(zhì)的特征峰與2小時的基本一致�����,表明水熱硫化反應(yīng)基本上在2小時內(nèi)結(jié)束���。
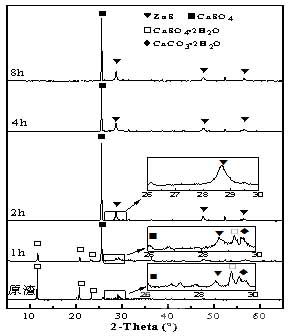
圖4 不同水熱硫化時間下重金屬硫化廢渣的XRD圖
2.3 水熱合成硫化鋅晶體結(jié)構(gòu)及生長規(guī)律的研究
圖3圖4均表明,雖然中和渣水熱硫化后產(chǎn)物的XRD圖譜上有較明顯的硫化鋅的特征峰��,但是特征峰出現(xiàn)了明顯的寬化現(xiàn)象���,一般認(rèn)為這是晶粒過細(xì)造成的[16]���。而礦物學(xué)通常認(rèn)為,過細(xì)的硫化物晶體難以通過浮選進(jìn)行回收[9]��。因此���,我們需要對水熱合成的硫化鋅晶體結(jié)構(gòu)及生長規(guī)律進(jìn)行探索���。
試驗在相同的水熱環(huán)境中�����,改變反應(yīng)溫度�����、時間���,對合成的ZnS產(chǎn)物進(jìn)行XRD分析。圖5為反應(yīng)時間4h��,反應(yīng)溫度分別為200℃���、220℃���、240℃、260℃��、280℃的系列樣品的XRD圖譜���,與標(biāo)準(zhǔn)立方相硫化鋅(JCPDS card�����,NO.05-0566)比較�����,我們可以看出���,200℃時,衍射譜中已出現(xiàn)了立方相硫化鋅的(111)(220)和(331)衍射峰���,但衍射峰強(qiáng)度較弱���,結(jié)晶不完全。當(dāng)反應(yīng)溫度逐漸升高時���,衍射峰強(qiáng)度逐漸增強(qiáng)��,峰形尖銳清晰���,說明樣品結(jié)晶程度隨反應(yīng)溫度提高而趨于完善。這是因為一般在較低溫度下��,結(jié)晶過程主要由表面反應(yīng)這一步控制,當(dāng)溫度升高時��,生長速度加快���,擴(kuò)散就逐漸成為控制結(jié)晶過程的主要步驟了[17]�����。在較高的溫度下生長的晶體���,由于結(jié)晶質(zhì)點排斥外來雜質(zhì)能力的增強(qiáng),其長出的晶體質(zhì)量一般要比較低溫度下生長的好[18]�����。
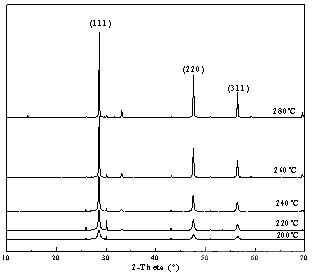
圖5 不同溫度下水熱合成的硫化鋅樣品的XRD圖譜
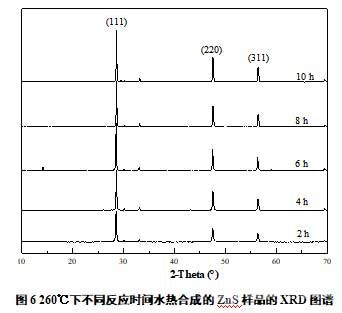
圖6為反應(yīng)溫度260℃��,反應(yīng)時間分別為2h�����、4h��、6h��、8h、10h的系列樣品的XRD圖譜���,由圖可知��,反應(yīng)時間為2h時���,已生成硫化鋅立方相��,只是主要衍射峰強(qiáng)度較弱���。這是由于晶化時間太短�����,反應(yīng)不夠充分�����,結(jié)晶狀況較差所致��。隨著反應(yīng)時間延長���,特征峰強(qiáng)度逐漸增強(qiáng)。這個過程是由于反應(yīng)前期生成硫化鋅不穩(wěn)定晶核,其數(shù)量隨時間的延長而增加并逐漸長大�����,當(dāng)晶核的尺寸大于臨界晶核尺寸時��,成為穩(wěn)定的晶核并開始生長[19]��。
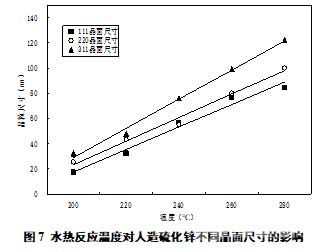
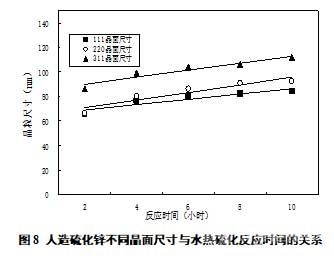
另外�����,通過謝樂公式對其晶粒尺寸進(jìn)行計算��,結(jié)果如圖7��、圖8所示�����。結(jié)果表明�����,人工合成的硫化鋅晶體各晶面的尺寸大小基本一致�����,晶體隨著時間或溫度的生長速度基本相同,說明人造硫化鋅與天然閃鋅礦同屬于等軸晶系�����,而正四面體狀生長基元是其有利基元[20]���。同時結(jié)果表明隨著反應(yīng)溫度的升高�����,或者反應(yīng)時間的延長,人工合成的硫化鋅晶體粒徑不斷增大���。例如當(dāng)溫度由200℃升高至260℃時���,硫化鋅晶粒尺寸可以由24.85nm增長為102.33nm;當(dāng)反應(yīng)時間由2小時延長至8小時時,硫化鋅晶粒尺寸可以由72.68nm增長為92.16nm���,說明延長反應(yīng)時間��、提升反應(yīng)溫度有利于硫化鋅晶粒的生長��,而晶粒大結(jié)晶性好的人造硫化物則有助于后續(xù)的浮選[21]��。
3 結(jié)論
水熱硫化技術(shù)處理重金屬廢渣是一種回收重金屬的新方法��,本文從水熱體系下硫元素賦存狀態(tài)��、中和渣水熱硫化過程特征�����、水熱合成硫化鋅晶體結(jié)構(gòu)及生長規(guī)律三個方面開展了相關(guān)基礎(chǔ)研究��,所得結(jié)論如下:
(1) 水熱條件下硫元素主要以S2-��、HS-���、SO42-等形式存在,其中HS-其主要的硫化作用��,溫度升高有利于重金屬的硫化反應(yīng)���。硫磺歧化產(chǎn)生的S2O32-會進(jìn)一步轉(zhuǎn)化為SO42-,而大量SO42-會使反應(yīng)體系的pH降低���,不利于硫化反應(yīng)��,反應(yīng)中必須保證廢渣中含有足量含鈣類等物質(zhì)與硫酸根離子進(jìn)行結(jié)合��。
(2) 中和渣水熱硫化過程的研究表明��,水熱反應(yīng)基本上在2小時內(nèi)結(jié)束��。廢渣中鋅的硫化最優(yōu)溫度為200℃以上。水熱過程首先發(fā)生的是硫磺的歧化反應(yīng),隨后是硫酸鈣晶體的生成��,最后是硫化鋅晶體的生成��。
(3) 水熱硫化產(chǎn)生的硫化鋅晶體與天然閃鋅礦一樣屬于等軸晶系�����,而正四面體狀生長基元是其有利基元�����,生長規(guī)律與天然閃鋅礦一致�����。然而粒徑較小是其與天然閃鋅礦的主要差別���。試驗表明,水熱反應(yīng)溫度的升高�����,反應(yīng)時間的延長,均有利于人工合成的硫化鋅晶體粒徑的長大�����,對后續(xù)的浮選回收有利。
參考文獻(xiàn)
[1] 孟祥和, 胡國飛. 重金屬廢水處理[M]. 北京: 化學(xué)工業(yè)出版社, 2000: 139-143.
[2] 劉清, 招國棟, 趙由才. 有色冶金廢渣中有價金屬回收的技術(shù)及現(xiàn)狀[J]. 有色冶金設(shè)計與研究, 2007, 23(28): 22-26.
[3] D Kuchar, T Fukuta, MS Onyango, et al. Sulfidation treatment of copper-containing plating sludge towards copper resource recovery[J]. Journal of Hazardous Materials, 2006. 138(1): 86-94.
[4] D Kuchar, T Fukuta, MS Onyango, et al. Sulfidation of zinc plating sludge with Na2S for zinc resource recovery[J]. Journal of Hazardous Materials, 2006, 137(1): 185-191.
[5] Li Yong, Wang Ji-kun, Wei Chang, et al. Sulfidation roasting of low grade lead-zinc oxide ore with elemental sulfur[J]. Minerals Engineering, 2010, 23(7): 563-566.
[6] F Rashchi, A Dashti, et al. Anglesite flotation: a study for lead recovery from zinc leach residue[J]. Minerals Engineering, 2005, 18(2): 205-212.
[7] Fa Keqing, Miller Jan, Jiang Tao, et al. Sulphidization flotation for recovery of lead and zinc from oxide-sulfide ores[J]. Transactions of Nonferrous Metals Society of China, 2005, 15(5): 1138-1144.
[8] Vanthuyne, M A Maes. The removal of heavy metals from contaminated soil by a combination of sulfidisation and flotation[J]. Science of the Total Environment, 2002, 269(1-3): 69-80.
[9] Miettinen, T J Ralston, D Fornasiero. The limits of fine particle flotation[J]. Minerals Engneering, 2010, 23: 420-437.
[10] Robb, LJ, ed. Introduction to ore-forming processes. 2005, Blackwell Science, Carlton, VIC, Australia.
[11] Masoud Salavati-Niasari, MRL-E, Fatemeh Davarb. Controllable synthesis of wurtzite ZnS nanorods through simple hydrothermal method in the presence of thioglycolic acid[J]. Journal of Alloys and Compounds, 2009, 475: 782–788.
[12] K Byrappa, T Adschiri. Hydrothermal technology for nanotechnology[J]. Progress in Crystal Growth and Characterization of Materials[J], 2007, 53: 117-166.
[13] Cheng Zhi-guo, Si Da-jie, Geng Bao-you. Controlled synthesis of copper sul?de 3D nanoarchitectures through a facile hydrothermal route[J]. Journal of Alloys and Compounds, 2010, 492: L44–L49.
[14] Liang Yan-Jie , CHAI Li-yuan, Liu Hui, et al. Hydrothermal suldation of zinc-containing neutralization sludge for zinc recovery and stabilization[J]. Minerals Engineering, 2012, 25: 14-19.
[15] 劉巽伯. 膠凝材料: 水泥、石灰��、石膏的生產(chǎn)和性能[M]. 上海: 同濟(jì)大學(xué)出版社, 1990: 17.
[16] Cullity, BD, ed. Elements of X-ray Diffraction second ed. 1997, Addison-Wesley.
[17] 仲維卓, 華素坤. 晶體生長形態(tài)學(xué)[M]. 北京: 科學(xué)出版社, 1999: 178.
[18] 馮儀, 馬天翼, 劉蕾等. 無機(jī)納米晶的形貌調(diào)控及生長機(jī)理研究[J].中國科學(xué), 2009.
[19] Kuppayee, M, GKV Nachiyar, and V Ramasamy, Synthesis and characterization of Cu2+ doped ZnS nanoparticles using TOPO and SHMP as capping agents[J]. Applied Surface Science, 2011, 257: 6779–6786.
[20] 施爾畏. 水熱結(jié)晶學(xué)[M]. 北京: 科學(xué)出版社, 2004.
[21] LIU Xiao-wen, HU Yue-hua, JIANG Hao, et al. Crystal structure and surface property of kaolinite in hard kaolins and soft kaolins. The Chinese journal of nonferrous metals, 2001, 11(4): 687-691.
聲明:
“重金屬廢渣水熱硫化回收金屬的基礎(chǔ)研究” 該技術(shù)專利(論文)所有權(quán)利歸屬于技術(shù)(論文)所有人。僅供學(xué)習(xí)研究���,如用于商業(yè)用途���,請聯(lián)系該技術(shù)所有人���。
我是此專利(論文)的發(fā)明人(作者)

 1824
編輯:中冶有色技術(shù)網(wǎng)
來源:中南大學(xué)冶金與環(huán)境學(xué)院
1824
編輯:中冶有色技術(shù)網(wǎng)
來源:中南大學(xué)冶金與環(huán)境學(xué)院









 分享 0
分享 0
 舉報 0
舉報 0
 收藏 0
收藏 0
 反對 0
反對 0
 點贊 0
點贊 0

 中冶有色技術(shù)平臺
中冶有色技術(shù)平臺 2024年12月27日 ~ 29日
2024年12月27日 ~ 29日  2025年01月03日 ~ 05日
2025年01月03日 ~ 05日  2025年01月03日 ~ 05日
2025年01月03日 ~ 05日  2025年01月03日 ~ 05日
2025年01月03日 ~ 05日  2025年04月27日 ~ 29日
2025年04月27日 ~ 29日 
